विद्युत आवेश - परिभाषा, सूत्र, गुण
इस लेख में हम आवेश (इलेक्ट्रिक चार्ज, Electric Charge) की परिभाषा, उसके गुण, सूत्र और उससे संबंधित नियम, आदि के बारे में जानेंगे।
 Table of Contents
Table of Contents- विद्युत आवेश क्या होता है?
- विद्युत आवेश के प्रकार
- किसी वस्तु को कैसे आवेशित किया जाता है?
- आवेश की इकाई
- इलेक्ट्रिक आवेश के गुण
विद्युत आवेश क्या होता है?
विद्युत आवेश या इलेक्ट्रिक चार्ज किसी भी पदार्थ का वह मूल गुण है, जिसके कारण वह विद्युत-चुंबकीय प्रभाव (electro-magnetic effects) उत्पन्न या अनुभव करता है।
जिस वस्तु में विद्युत आवेश होता है, उसे विद्युतीकृत या आवेशित कहा जाता है। जब किसी वस्तु पर कोई आवेश नहीं होता है, तो उसे तटस्थ या आवेशरहित कहा जाता है।
विद्युत आवेश के प्रकार
मूल रूप से दो प्रकार के विद्युत आवेश होते हैं:
- सकारात्मक आवेश या धन आवेश (Positive Charge), जैसे एक प्रोटॉन का आवेश
- नकारात्मक आवेश या ऋण आवेश (Negative Charge), जैसे इलेक्ट्रॉन का आवेश
धन आवेश और ऋण आवेश शब्द, अमेरिकी वैज्ञानिक बेंजामिन फ्रैंकलिन (Benjamin Franklin) द्वारा गढ़े गए थे।
 नोट
नोटहो सकता है की किसी पदार्थ पर कोई आवेश नहीं हो, अर्थात वह आवेशरहित हो सकता है। सभी पदार्थों के लिए धनात्मक या ऋणात्मक आवेशित होना आवश्यक नहीं है।
यह दो प्रकार के विद्युतीकरण प्रभावों को जन्म देता है।
- समान आवेश एक दूसरे को प्रतिकर्षित (repel) करते हैं - अतः दो धनात्मक आवेश एक दूसरे को प्रतिकर्षित करते हैं। साथ ही, दो ऋणात्मक आवेश एक दूसरे को प्रतिकर्षित करते हैं। उदाहरण के लिए, यदि आप दो इलेक्ट्रॉनों को एक साथ रखते हैं, तो वे एक दूसरे से दूर चले जाएंगे।
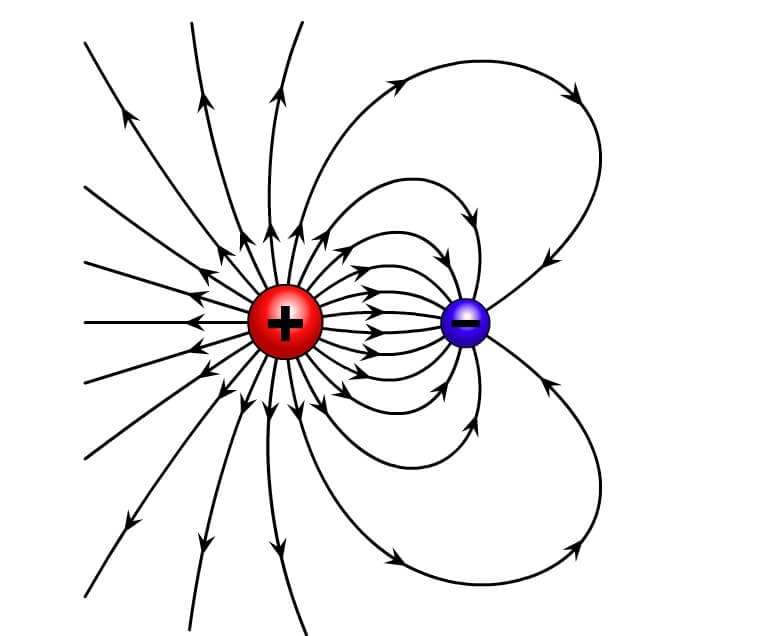
- विपरीत आवेश एक-दूसरे को आकर्षित (attract) करते हैं - अतः धनात्मक और ऋणात्मक आवेश एक-दूसरे को आकर्षित करेंगे। उदाहरण के लिए, यदि आप एक इलेक्ट्रॉन और एक प्रोटॉन को एक साथ रखते हैं, तो वे एक दूसरे की ओर बढ़ेंगे।
जब समान धनात्मक और ऋणात्मक आवेश मिलते हैं, तो वे एक दूसरे को आवेशरहित कर देते हैं।
किसी वस्तु को कैसे आवेशित किया जाता है?
यह लंबे समय तक रहस्य बना रहा। जब तक बेंजामिन फ्रैंकलिन ने धन आवेश और ऋण आवेश की अवधारणाएं नहीं दे दीं।
एक वस्तु को दो तरह से विद्युतीकृत किया जा सकता है:
- यह धनात्मक रूप से आवेशित हो सकता है, या तो धनात्मक आवेशित कण प्राप्त करके, या ऋणात्मक आवेशित कण को खोकर।
- यह ऋणात्मक रूप से आवेशित हो सकता है, या तो ऋणात्मक आवेशित कण प्राप्त करके, या धनात्मक आवेशित कण को खोकर।
हालांकि, इलेक्ट्रॉनों को खोना या प्राप्त करना वह सबसे आम तरीका है, जिससे विभिन्न वस्तुएं चार्ज/विद्युतीकृत होती हैं।
चूंकि इलेक्ट्रॉन ऋणात्मक आवेश वाले होते हैं, इसलिए जो पिंड इलेक्ट्रॉनों को ग्रहण करता है वह ऋणात्मक रूप से आवेशित हो जाता है और जो पिंड इलेक्ट्रॉनों को खो देता है वह धनात्मक आवेशित हो जाता है।
किसी वस्तु को आवेशित होने के लिए जितने इलेक्ट्रॉनों की आवश्यकता होती है, वह उनके शरीर में इलेक्ट्रॉनों की कुल संख्या की तुलना में बहुत कम होते हैं।
 स्थैतिक बिजली
स्थैतिक बिजलीकिसी पदार्थ के कुछ ढीले-ढाले इलेक्ट्रॉनों को केवल रगड़ने से भी दूसरे पदार्थ में स्थानांतरित किया जा सकता है।
क्या आपने कभी स्थैतिक बिजली (Static Electricity) के झटके का अनुभव किया है? कभी-कभी, हमें किसी पदार्थ को छूने मात्र से स्थैतिक बिजली का झटका लगता है। यहां तक कि कुछ मामलों में चिंगारी भी देखी जा सकती है।
लगभग 600 ईसा पूर्व ग्रीस में, Thales of Miletus (मिलेटस के थेल्स) ने एम्बर (amber) को ऊन या रेशमी कपड़े से रगड़ा। उन्होंने देखा कि एम्बर ने कुछ अद्वितीय गुण प्राप्त कर लिए हैं - यह हल्के वजन की वस्तुओं को अपनी ओर आकर्षित करना शुरू कर देता है। उन्होंने मूल रूप से जो किया था, वह एम्बर को रगड़ कर चार्ज या विद्युतीकृत करना था। यह स्थैतिक बिजली है।
वास्तव में, इलेक्ट्रिसिटी (Electricity) शब्द एक ग्रीक शब्द Elektron से आया है, जिसका अर्थ एम्बर है।
आवेश की इकाई
पदार्थ के अन्य गुणों की तरह, हम आवेश को भी माप सकते हैं। इस उद्देश्य के लिए, हम विभिन्न इकाइयों का उपयोग करते हैं।
कूलम्ब
इंटरनेशनल सिस्टम ऑफ यूनिट्स (SI) में, आवेश की एक इकाई को कूलम्ब (Coulomb) कहा जाता है। इसे चिन्ह C से निरूपित करते हैं।
हालाँकि, कूलम्ब एक बड़ी इकाई है। इसलिए, इलेक्ट्रोस्टैटिक्स में हम अक्सर माइक्रो कूलम्ब (μC) या मिली कूलम्ब (mC) की छोटी इकाई का उपयोग करते हैं।
- 1 μC = 10-6 C
- 1 mC = 10-3 C
आवेश की मूल इकाई (e)
1 इलेक्ट्रॉन या प्रोटॉन पर स्तिथ आवेश को, आवेश की मूल इकाई माना जाता है।
- एक प्रोटॉन पर आवेश +e के रूप में दर्शाया जाता है
- एक इलेक्ट्रॉन पर आवेश को -e के रूप में दर्शाया जाता है
-1 कूलम्ब का आवेश बनाने के लिए हमें 6 × 1018 इलेक्ट्रॉनों की आवश्यकता होती है।
तो, 1 इलेक्ट्रॉन, यानी e का आवेश 1.602192 × 10-19 C होता है।
यही बात प्रोटॉन पर भी लागू होती है।
1 कूलम्ब का आवेश बनाने के लिए हमें 6 × 1018 प्रोटॉन की आवश्यकता होती है (या हमें इतने सारे इलेक्ट्रॉनों को खोने की आवश्यकता होती है)।
अतः 1 प्रोटॉन, अर्थात e का आवेश 1.602192 × 10-19 C होता है।
सामान्य तौर पर, वस्तुएं आमतौर पर प्रोटॉन प्राप्त करने के बजाय अपने इलेक्ट्रॉनों को खोकर धनात्मक आवेश प्राप्त करती हैं। कुछ परमाणु आसानी से इलेक्ट्रॉनों को खो सकते हैं। इसके विपरीत, प्रोटॉन प्राप्त करना या खोना इतनी सरल प्रक्रिया नहीं है।
 कूलम्ब की परिभाषा
कूलम्ब की परिभाषायदि हम किसी तार में से 1 सेकंड के लिए 1 एम्पीयर की विद्युत धारा चलाते हैं, तो एक कूलम्ब का आवेश प्रवाहित होता है।
अब, आइए आवेशों से संबंधित कुछ अन्य बुनियादी गुणों पर एक नज़र डालते हैं।
इलेक्ट्रिक आवेश के गुण
आवेश एक अदिश राशि है
आवेश एक अदिश राशि (scalar quantity) है, जिसका अर्थ है कि इसमें केवल परिमाण (magnitude) होता है, कोई दिशा नहीं होती है।
हालांकि, यह द्रव्यमान (mass) जैसे कुछ अन्य पदार्थ गुणों से थोड़ा अलग है। द्रव्यमान भी आवेश की तरह ही एक अदिश राशि है। दोनों में परिमाण है, लेकिन दिशा नहीं है। लेकिन द्रव्यमान ऋणात्मक नहीं हो सकता। जबकि आवेश धनात्मक या ऋणात्मक दोनों हो सकता है।
 नोट
नोटआप लोगों ने एंटीमैटर (Antimatter) के बारे में तो सुना ही होगा। जब पदार्थ (matter) और एंटीमैटर एक साथ आते हैं तो द्रव्यमान नष्ट हो जाता है और शुद्ध ऊर्जा उत्पन्न होती है।
हालांकि, इसका मतलब यह नहीं है कि एंटीमैटर का द्रव्यमान नकारात्मक होता है। कम से कम जिस ब्रह्मांड में हम रहते हैं, उसमें नकारात्मक द्रव्यमान जैसी कोई चीज नहीं है। द्रव्यमान हमेशा सकारात्मक होता है।
आवेश एक दूसरे में जुड़ सकते हैं या समाप्त हो सकते हैं
यदि किसी निकाय/सिस्टम में कई आवेश हैं, तो हम कुल आवेश को खोजने के लिए उन्हें बीजगणितीय रूप से जोड़ सकते हैं।
अतः, यदि किसी निकाय में n आवेश q1, q2, q3, …, qn हैं, तो:
निकाय का कुल आवेश = q1 + q2 + q3 + … + qn
 नोट
नोटजब हम कहते हैं कि हमें बीजगणितीय रूप से जोड़ने की आवश्यकता है, तो हमारा मतलब है कि हमें धनात्मक और ऋणात्मक चिन्हों को ध्यान में रखना होगा।
आवेश का परिमाणीकरण (Quantization of Charge)
सभी आवेश, आवेश की मूल इकाई के अभिन्न गुणज होते हैं। तो, किसी निकाय में कुल आवेशों (q) को इस प्रकार दर्शाया जा सकता है:
q = ne
जहाँ n कोई पूर्णांक है, धनात्मक या ऋणात्मक।
 नोट
नोटआवेश का परिमाणीकरण सबसे पहले फैराडे (Faraday) द्वारा सुझाया गया था। इसे 1912 में मिलिकन (Millikan) द्वारा प्रयोगात्मक रूप से सिद्ध किया गया था।
आवेशों के संरक्षण का कानून
यदि किसी निकाय को अलग कर दिया जाता है (isolated), तो उसके भीतर कुल आवेश वही रहेगा। वह बढेगा या घटेगा नहीं| यह आवेशों के संरक्षण का नियम (law of Conservation of Charges) है।